
国家局创新医疗器械产品注册特别审查申请办理条件如下:
1.《创新医疗器械特别审批程序(试行)》(食药监械管〔2014〕13号)第四条:“第四条 申请人申请创新医疗器械特别审批,应当填写《创新医疗器械特别审批申请表》(见附件1),并提交支持拟申请产品符合本程序第二条要求的资料。资料应当包括:
(一)申请人企业法人资格证明文件。
(二)产品知识产权情况及证明文件。
(三)产品研发过程及结果的综述。
(四)产品技术文件,至少应当包括:
1.产品的预期用途;
2.产品工作原理/作用机理;
3.产品主要技术指标及确定依据,主要原材料、关键元器件的指标要求,主要生产工艺过程及流程图,主要技术指标的检验方法。
(五)产品创新的证明性文件,至少应当包括:
1.信息或者专利检索机构出具的查新报告;
2.核心刊物公开发表的能够充分说明产品临床应用价值的学术论文、专著及文件综述;
3.国内外已上市同类产品应用情况的分析及对比(如有);
4.产品的创新内容及在临床应用的显著价值。
(六)产品安全风险管理报告。
(七)产品说明书(样稿)。
(八)其他证明产品符合本程序第二条的资料。
(九)境外申请人应当委托中国境内的企业法人作为代理人或者由其在中国境内的办事机构提出申请,并提交以下文件:
1.境外申请人委托代理人或者其在中国境内办事机构办理创新医疗器械特别审批申请的委托书;
2.代理人或者申请人在中国境内办事机构的承诺书;3.代理人营业执照或者申请人在中国境内办事机构的机构登记证明。
(十)所提交资料真实性的自我保证声明。申报资料应当使用中文。原文为外文的,应当有中文译本。”
国家局创新医疗器械注册特别审查流程
(一)境内申请人应当向其所在地的省级药品监督管理部门提出创新医疗器械特别审查申请。省级药品监督管理部门对申报项目是否符合本程序第二条要求进行初审,并于20个工作日内出具初审意见。经初审不符合第二条要求的,省级药品监督管理部门应当告知申请人;符合第二条要求的,省级药品监督管理部门将申报资料和初审意见一并报送国家药品监督管理局行政事项受理服务和投诉举报中心。境外申请人应当向国家药品监督管理局提出创新医疗器械特别审查申请。受理和举报中心对创新医疗器械特别审查申请申报资料进行形式审查,对符合本程序第四条规定的形式要求的予以受理。
(二)国家药品监督管理局医疗器械技术审评中心设立创新医疗器械审查办公室,对创新医疗器械特别审查申请进行审查。创新医疗器械审查办公室收到创新医疗器械特别审查申请后,组织专家进行审查,应当于60个工作日内出具审查意见(公示及异议处理时间不计算在内)。
(三)经创新医疗器械审查办公室审查,对拟进行特别审查的申请项目,应当在器审中心网站将申请人、产品名称予以公示,公示时间应当不少于10个工作日。对于公示内容有异议的,应当对相关意见研究后作出最终审查决定。创新医疗器械审查办公室作出审查决定后,将审查结果通过器审中心网站告知申请人。
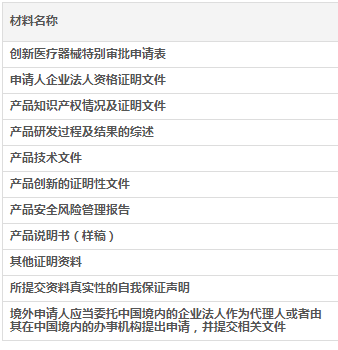
国家局创新医疗器械产品注册办理特别审查材料目录:
鸿远医疗器械咨询服务公司 是一家技术专业的医疗器械咨询服务公司,专注提供全国各地如:深圳、广州、东莞、中山、佛山、潮州、顺德、上海、西安、重庆、成都、安徽、江苏、浙江等知名城市的医疗器械领域技术咨询服务。鸿远医疗器械咨询专业服务于:医疗器械注册证代办理咨询、医疗器械产品分类界定代办理,代办医疗器械生产许可证、一类医疗器械产品备案代办、体外诊断试剂注册、进口医疗器械注册、医疗器械经营许可证代办、二类医疗器械经营备案、CE认证、ISO13485认证、FDA注册、FDA认证、临床试验、医疗器械质量管理体系认证及体系建立与过程确认文件建立( ISO13485, GMP, CE,QSR820,CMDCAS);注册、医疗器械出口销售证明、产品技术要求制订、技术文件、同类产品对比免临床评价资料编写、注册资料编写辅导、医疗器械广告批文申报、电磁兼容整改等提供一站式服务公司,欢迎您咨询与合作!

 在线客服
在线客服