
医疗器械注册证申请牙科手机产品的命名应采用《医疗器械通用名称命名规则》(国家食品药品监督管理总局令第19号)或国家标准、行业标准上、医疗器械通用名称为依据。
1.若牙科手机的申报组成中包含牙科弯手机和牙科直手机,应使用“牙科手机”作为注册产品名称;若牙科手机仅为单独的牙科弯手机或牙科直手机,应使用“牙科弯手机”或“牙科直手机”作为注册产品名称。
2.医疗器械产品注册证申报高速气涡轮手机应规范使用“高速气涡轮手机”作为产品名称。
产品的结构和组成
1.牙科手机的结构组成
例如高速气涡轮手机:由高速气涡轮手机和接头(若有)组成;
2.术语解释
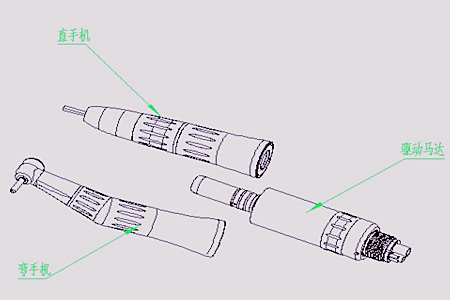
(1)牙科手机:用于向牙科工具或器具传递(带转换或不带转换)工作所需能量的手持工具。
(2)弯手机:主轴与被夹工具或器具呈角度的牙科手机,其输入轴与输出轴之间具有角度。牙科手机的一种结构方式。
(3)直手机:用来向器具传递和/或转换旋转运动的手机,其轴与手机主轴相重合。牙科手机的一种结构方式。
(4)照明方式分为带照明装置式、导光式、无照明式三种方式。
①带照明装置式:牙科手机结构中含照明光源。
②导光式:牙科手机结构不含照明光源,但结构中含有导光装置。照明光源通过可弯曲的导光纤维束(玻璃或石英)传导外部照明光源提供的光照。该导光装置可射出光束,直接导向所需区域。
③无照明式:牙科手机结构既不含照明光源,又不带导光装置。
3.医疗器械注册证代理结构/组成描述
(1)机头:机头是牙科高速气涡轮手机的核心功能区,是夹持车针、水、工作气、回气,光源各功能汇集处。
经过过滤和调压(额定值)的压缩空气分两路进入,一路作为驱动气体,一路作为冷却气体。
经过过滤和调压(额定值)的自来水(纯净水)作为冷却水进入机头。
如是光纤手机还有导光棒进入机头。
(2)手柄:手柄中空管状,密封。细端与机头连接,粗端与接头(或快速接头)连接。
中间有水管、气管、导光棒(如有)通过。
手柄本身是手机回气管的一部分。
(3)接头(或快速接头):接头(或快速接头)是手机连接外部气、水、电源的对接口,有两孔、三孔、四孔、五孔、六孔、八孔之分。
(4)直手机:机头是核心功能区,是夹持车针、水、气、光源各功能汇集处,中间有动力传动机构、水管、气管、导光棒(如有)通过,尾部有动力连接器与驱动马达连接,接受来自于驱动马达的旋转动力。直手机的设计应符合人机工程学原理。外型平滑便于清洁和消毒。
(5)弯手机:机头是核心功能区,是夹持车针、水、气、光源各功能汇集处,中间有动力传动机构、水管、气管、导光棒(如有)通过,尾部有动力连接器与驱动马达连接,接受来自于驱动马达的旋转动力。手机的设计应符合人机工程学原理。外型平滑便于清洁和消毒。
4.医疗器械产品注册证代理申报产品牙科手机控制系统:
牙科手机一般没有控制系统,只有简单的水、气、光源调节装置。
产品工作原理/作用机理
牙科手机是一种口腔治疗器械,由整体或成套相互关联的器械部件所组成。
医疗器械注册证办理单元划分的原则和实例
1.高速气涡轮手机、牙科弯手机/牙科直手机应划分为不同的注册单元。
2.牙科弯手机/牙科直手机中夹持根管锉用于扩大牙齿根管的手机、用于口腔种植治疗的手机、用于牙齿钻孔打磨用的手机应划分为不同的注册单元。
3.带照明装置式的手机与无照明式的手机应划分为不同的注册单元;导光式与无照明式的手机可放在同一注册单元。
医疗器械注册证代办产品适用的相关标准具体相关的常用标准列举如下:
标准编号标准名称
GB 9706.1—2007医用电气设备第1部分:安全通用要求
GB/T 191—2008包装贮运图示标志
GB/T 9937.3—2008口腔词汇第3部分:口腔器械
GB/T 14710—2009医用电器设备环境要求及试验方法
YY 1012—2004牙科手机联轴节尺寸
YY 1045.1—2009牙科手机第1部分:高速气涡轮手机
YY 1045.2—2010牙科手机第2部分:直手机和弯手机
YY 0505—2012医用电气设备第1—2部分:安全通用要求并列标准:电磁兼容要求和试验
YY/T 0514—2009牙科手机软管连接件
GB/T 16886.1—2011医疗器械生物学评价第1部分:风险管理过程中的评价与试验
YY/T 0268—2008牙科学口腔医疗器械生物学评价第1单元:评价与试验
ISO 1797—1:2011牙科旋转器械杆第1部分:金属杆
ISO 1797—2:1992牙科旋转器械杆第2部分:塑料杆
ISO 13402:1995外科和牙科手持器械耐蒸汽消毒、耐腐蚀和耐热性能的测试
上述标准包括了医疗器械注册产品标准中经常涉及到的标准。有的企业还会根据产品的特点引用一些行业外的标准和欧盟及一些较为特殊的标准。
对产品适用及引用标准的审查可以分三步来进行。
医疗器械产品注册证代办首先对引用标准的齐全性和适宜性进行审查,也就是在编写产品技术要求时是否引用了与产品相关的国家标准、行业标准,以及引用是否准确。应注意标准编号、标准名称是否完整规范,年代号是否有效。
其次对引用标准的采纳情况进行审查。即所引用的标准中的条款要求,是否在产品技术要求中进行了实质性的条款引用。这种引用通常采用两种方式,文字表述繁多内容复杂的可以直接引用标准及条文号,比较简单的也可以直接引述具体要求。
医疗器械产品注册证办理如有新版强制性国家标准、行业标准发布实施,产品性能指标等要求应执行最新版本的国家标准、行业标准。
鸿远医疗器械咨询服务公司 是一家技术专业的医疗器械咨询服务公司,专注提供全国各地如:深圳、广州、东莞、中山、佛山、潮州、顺德、上海、西安、重庆、成都、安徽、江苏、浙江等知名城市的医疗器械领域技术咨询服务。鸿远医疗器械咨询专业服务于:医疗器械产品注册证办理咨询、医疗器械产品分类界定代办理,代办医疗器械生产许可证、一类医疗器械产品备案代办、医疗器械经营许可证代办、二类医疗器械经营备案、进口医疗器械注册、CE认证、ISO13485认证、FDA注册、FDA认证、临床试验、医疗器械质量管理体系认证及体系建立与过程确认文件建立(ISO9001, ISO13485, GMP, CE,QSR820,CMDCAS);注册、出口证、自由销售证办理、产品技术要求制订、技术文件、临床试验及免临床同类产品对比资料编写、注册资料编写辅导、电磁兼容整改、医疗器械广告批文申报等提供一站式服务公司,欢迎您咨询与合作!

 在线客服
在线客服