
医疗器械注册医用激光光纤产品技术要求范例:
本部分内容给出需要考虑的产品主要技术指标,如有其他附加功能,注册申请人应根据产品性能结构特点,参考相应的国家标准、行业标准,增加相关要求。
医疗器械产品注册技术要求编号:
一次性使用无菌激光光纤(示例)
1. 产品型号/规格及其划分说明
1.1 产品型号:
1.1.1 命名规则:
1.1.2基本参数:
a)总长度
b)纤芯直径
c)光纤适用的波长
d)对应波长的最低传输效率
e)预期使用时最大传输功率/能量
f)清洗、消毒或灭菌方法
g)抗拉强度
h)光纤最小弯曲工作半径/直径
i)连接器类型
1.1.3 配合光纤使用的主机
专用型光纤应明确配合使用主机的厂商信息及主机性能要求信息。
通用型光纤应明确配合使用主机的性能要求信息。
1.2 划分说明
2. 性能指标
2.1 光纤性能
2.1.1 光纤长度
2.1.2 纤芯直径
2.2光学性能
2.2.1光纤传输效率
光纤平直放置时对xxx nm波长的激光传输效率应不小于xx。
若光纤可以传输多个波长,则应明确每个波长对应的传输效率。
2.2.2光纤传输效率不稳定度
2.2.3光纤传输效率复现性
2.3机械性能
2.3.1光纤抗拉强度
光纤传输体与连接器接合处、光纤传输体与外接治疗头(外接应用端、特殊处理的头端)接合处的抗拉强度均应不小于xx N。抗拉试验后,光纤传输效率应不小于试验前的90%。
2.3.2光纤最小弯曲工作半径
光纤最小弯曲工作半径为xx mm,当被弯曲至该值后,光纤传输效率应不小于试验前的90%。
2.3.3光纤弯曲抗疲劳性
光纤在最小弯曲工作半径条件下应能反复弯曲100次。弯曲抗疲劳试验后,光纤传输效率应不小于试验前的90%。
2.4外观:
光纤表面应光滑,无锋棱、毛刺和裂痕。各部件连接紧凑,不易剥落。
2.5环氧乙烷残留量
使用环氧乙烷灭菌的光纤,环氧乙烷残留量应不大于0.1mg/根。
2.6无菌
采用无菌包装的光纤应无菌。
2.7 发散角
对应波长的发散角:xx mrad,误差:±20%。
光纤为平切直射,应明确发散角。若应用端有特殊结构,应根据产品自身特点做出相应要求。例如,用于光动力治疗,还应符合YY0845中5.5的要求。若球形端对激光束有聚焦作用,则应在技术要求中明确焦距及焦点处光斑大小。
2.8医疗器械注册办理安全性能
电气安全要求:电气安全性能符合GB 9706.1-2007的相关要求。
电磁兼容要求:电磁兼容全面执行《YY 0505-2012 医用电气设备第1-2部分:安全通用要求 并列标准:电磁兼容要求和试验》标准(若适用)。
3. 医疗器械注册代办产品检验方法
在检验方法中应明确试验时的工作条件。如下:
试验条件:
(1)温度:
(2)湿度:
(3)大气压力:
医疗器械产品注册办理性能指标中的每条要求均应有相应的检测方法,并尽量保持检验方法中的编号与性能指标的编号对应。
附录A(示例)
1.产品特征
a)按防电击类型分类:不适用
b)按防电击的程度分类:无应用部分/B型应用部分/BF型应用部分/CF型应用部分
c)按对进液的防护程度分类:不适用(若适用,则应明确)
d)按在与空气混合的易燃麻醉气或与氧或氧化亚氮混合的易燃麻醉气情况下使用时的安全程度分类:不适用
e)按运行模式分类: 不适用
f)设备的额定电压和频率:不适用
g)设备的输入功率:不适用
h)设备具有对除颤放电效应防护的应用部分:不适用
i)设备具有信号输出和输入部分:不适用
j)非永久性安装设备:不适用
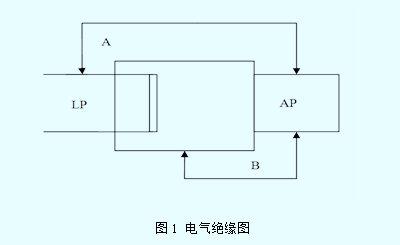
k)电气绝缘图(以BF型为例)
医疗器械注册代理注:不适用项可不写,注明适用项即可。
表A.1 电气绝缘表(以BF型为例)
| 编号 | 绝缘类型 | 参考电压 | 试验电压 |
| A | 加强绝缘(B-a) | 220V | 4000V |
| B | 基本绝缘(B-d) | 220V | 1500V |
附录B
1.激光光纤结构外观图。有多个型号的应提供每个型号的外观图。若外观无明显差异,可提供一张典型性产品的外观图。
2.提供图示说明光纤发光部位和发光方式
例如:
发光部位:光纤末端
发光方式:直射
3.材质:
明确纤芯、包层、涂覆层的材质。若产品还有其他部件,也应明确各部件的材质,尤其是接触患者部分的材质。
深圳鸿远医疗器械咨询服务公司 是一家技术专业的医疗器械咨询服务公司,专注提供全国各地如:深圳、广州、东莞、中山、佛山、潮州、顺德、上海、西安、重庆、成都、安徽、江苏、浙江等知名城市的医疗器械领域技术咨询服务。鸿远医疗器械咨询专业服务于:医疗器械产品注册代办理咨询、代办医疗器械生产许可证、一类医疗器械产品备案代办、医疗器械经营许可证代办、二类医疗器械经营备案、进口医疗器械注册、CE认证、ISO13485认证、FDA注册、FDA认证、临床试验、医疗器械质量管理体系认证及体系建立与过程确认文件建立(ISO9001, ISO13485, GMP, CE,QSR820,CMDCAS);注册、出口证、自由销售证办理、产品技术要求制订、技术文件、临床试验及免临床同类产品对比资料编写、注册资料编写辅导、电磁兼容整改、医疗器械广告批文申报等提供一站式服务公司,欢迎您咨询与合作!

 在线客服
在线客服