
医疗器械生产许可证延续办理《承诺制审批》条件:从事医疗器械生产活动,应当具备下列条件:(一)有与生产的医疗器械相适应的生产场地、环境条件、生产设备以及专业技术人员;(二)有能对生产的医疗器械进行质量检验的机构或者专职检验人员以及检验设备;(三)有保证医疗器械质量的管理制度;(四)有与生产的医疗器械相适应的售后服务能力;(五)符合产品研制、生产工艺文件规定的要求。
2023年医疗器械生产许可证延续办理流程《承诺制审批》
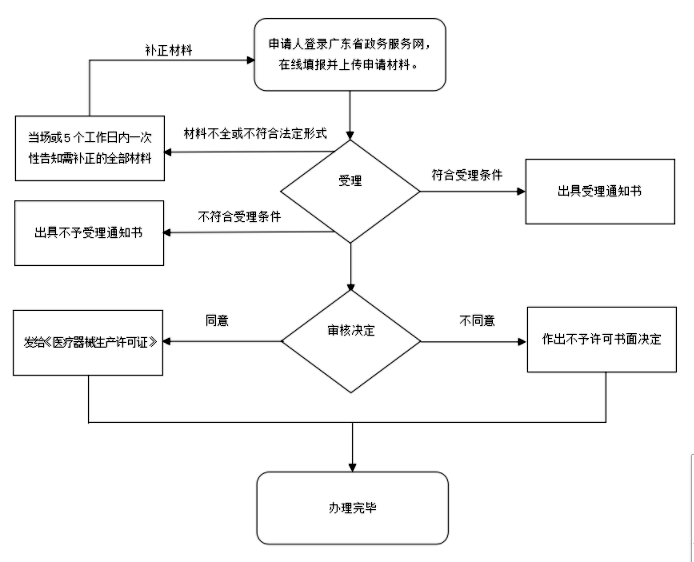
医疗器械生产许可证延续办理《承诺制审批》申请材料如下:
1、医疗器械生产许可证延续申请表
2、所生产的医疗器械注册证以及产品技术要求复印件
3、法定代表人(企业负责人)身份证明复印件
4、生产、质量和技术负责人的身份、学历、职称复印件
5、生产管理、质量检验岗位从业人员学历、职称一览表
6、生产场地的相关文件复印件,有特殊生产环境要求的,
还应当提交设施、环境的相关文件复印件。
7、主要生产设备和检验设备目录
8、质量手册和程序文件目录
9、生产工艺流程图
10、证明售后服务能力的材料
11、经办人的授权文件
12、一年内在相同生产地址且同属分类目录二级产品类别的产品通过体系核查的文件。
医疗器械生产许可证延续申请需要多长时间?
《医疗器械监督管理条例》中华人民共和国国务院令第739号,第三十二条第一款、第二款、第三款,从事第二类、第三类医疗器械生产的,应当向所在地省、自治区、直辖市人民政府药品监督管理部门申请生产许可并提交其符合本条例第三十条规定条件的有关资料以及所生产医疗器械的注册证。 受理生产许可申请的药品监督管理部门应当对申请资料进行审核,按照国务院药品监督管理部门制定的医疗器械生产质量管理规范的要求进行核查,并自受理申请之日起20个工作日内作出决定。对符合规定条件的,准予许可并发给医疗器械生产许可证;对不符合规定条件的,不予许可并书面说明理由。 医疗器械生产许可证有效期为5年。有效期届满需要延续的,依照有关行政许可的法律规定办理延续手续。
鸿远医疗器械咨询服务公司 是一家技术专业的医疗器械咨询服务公司,专注提供全国各地如:深圳、广州、东莞、中山、佛山、潮州、顺德、广西、上海、西安、重庆、成都、安徽、江苏、浙江等知名城市的医疗器械领域技术咨询服务。鸿远医疗器械咨询专业服务于:医疗器械产品注册证代办理咨询、医疗器械产品分类界定代办理,代办医疗器械生产许可证、一类医疗器械产品备案代办、体外诊断试剂注册、进口医疗器械注册、医疗器械经营许可证代办、二类医疗器械经营备案、CE认证、ISO13485认证、FDA注册、FDA认证、临床试验、医疗器械质量管理体系认证及体系建立与过程确认文件建立( ISO13485, GMP, CE,QSR820,CMDCAS);注册、医疗器械出口销售证明、产品技术要求制订、技术文件、同类产品对比免临床评价资料编写、注册资料编写辅导、医疗器械广告批文申报、电磁兼容整改等提供一站式服务公司,老师微信及手机号:13590396780欢迎您咨询与合作!

 在线客服
在线客服